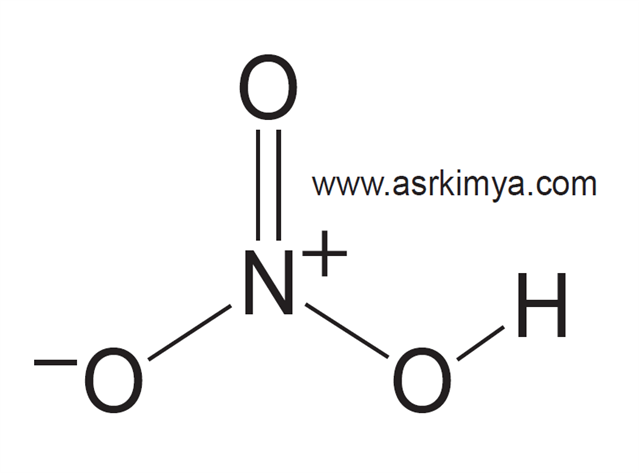
NİTRİK ASİT

GENEL
BİLGİLER
Kimyasal
Adı Nitric
Acid
Kimyasal
Formülü HNO3
Molekül
Ağırlığı 63.012 g / mol
CAS
Numarası 7697-37-2
Erime
Noktası -42 ° C (-44 °F; 231 K)
Kaynama
Noktası 83 ° C
Yoğunluk 1.51 g/cm3 (20
°C)
DİĞER
İSİMLERİ
• NITRIC ACID
• Azotik Asit
• Nitril hidroksit
• Nitrik Asit
• Salpetersaeure
• 7697-37-2
• Azotic acid
• Salpetersaeure
• Aqua fortis
• Red fuming nitric acid
• Nital
• Acide nitrique
• Acidum nitricum
• Nitricum acidum
• Nitrous fumes
• Nitryl hydroxide
• HNO3
• Salpetersaure
• RFNA
• Acido nitrico
• Azotowy kwas
• Kyselina dusicne
• Salpeterzuuroplossingen
• Nitric acid, anhydrous
NASIL
ÜRETİLİR
Nitrik
asit üretimi, Alman kimyager Wilhelm Ostwald'ın adını taşıyan ostwald süreci
ile yapılmaktadır. Amonyağın ostwald işlemi yoluyla oksidasyonu ile üretilir.
Nitrik asit, nitrojen dioksitin (NO2) su ile reaksiyona girmesi ile
oluşur. Aşırı derecede aşındırıcı ve zehirlidir. Nitrik asit, güçlü bir
oksitleyici ajandır. Çözelti içinde kolayca iyonlaşarak iyi bir elektrik
iletkeni oluşturur. Metaller, oksitler ve hidroksitlerle reaksiyona girerek nitrat
tuzları oluşturur.
FİZİKSEL
VE KİMYASAL ÖZELLİKLERİ
• Moleküler formülü HNO3’tür.
• Moleküler ağırlığı yaklaşık 63.01
g/mol’dür.
• Renksiz veya hafif sarımsı, dumanlı
sıvı görünüme sahiptir.
• Keskin, boğucu (asetik asit benzeri)
kokusu vardır.
• 25°C’de yoğunluğu yaklaşık 1.51 g/cm³
(konsantre formda)
• Erime noktası -42 °C
• Kaynama noktası 83 °C (saf HNO3)
• Suda tamamen çözünür (egzotermik
çözünme)
• pH değeri ~1 (1 M çözeltide)
• Yanıcı değildir ancak oksitleyici
olduğundan yanıcı maddelerle birlikte tehlike yaratabilir.
• Nitrik asit saf olduğunda renksizdir
ve dumanlıdır ancak bekletilirse azot oksitlerin toplanması sonucu sarımsı bir
görünüme sahip olur.
• Metaller veya dokular için oldukça
aşındırıcı sıvı bir mineral asittir.
• Zehirlidir ve ciddi yanıklara neden
olabilir.
• Buruk, boğucu kokuya sahiptir.
• Nitrik asit kararsızdır, ısı ile temas
ettiğinde ve ışığa, suya, nitrojen dioksit ve oksijene maruz kaldığında
ayrışır.
• -42 °C erime noktasına ulaşırken, 83
°C kaynama noktasına ulaşır.
• Nitrik asit, demir, bakır ve gümüş
gibi metalleri çözer.
• Uçucu ve havada sarımsı dumanlar
çıkarabilir.
• Güçlü bir asittir. Tamamen iyonlaşarak
H+ ve NO3- iyonlarına ayrışır.
• Oksitleyici özelliktedir, özellikle
metallerle tepkimeye girerek oksidasyon yapar. Aktif metallerle H2
gazı çıkararak reaksiyona girer. Soy metallerle (örneğin altın, platin)
genellikle tepkime vermez. Ancak “kral suyu” (HNO3 + HCl) bu
metaller üzerinde etkilidir.
• Proteinlerle ve organik maddelerle
şiddetli tepkime verebilir.
• Aromatik bileşiklerle nitrasyon
reaksiyonları gerçekleştirir.
• Işıkta bozulur. Işık ve ısı etkisiyle
azot dioksit (NO2) açığa çıkar, bu da renginin sararmasına neden
olur.
• Patlayıcı bileşiklerle reaksiyona
girebilir. Özellikle gliserin, aseton gibi maddelerle birleştiğinde patlayıcı
nitrat esterleri oluşturabilir.
KULLANIM
ALANLARI
• Gübre üretimi en büyük kullanım
alanıdır. Özellikle amonyum nitrat (NH4NO3) üretiminde
kullanılır.
• Patlayıcı madde üretiminde kullanılır.
TNT (trinitrotoluen), nitrogliserin, pikrik asit gibi patlayıcı maddelerin
sentezinde görev alır.
• Askerî ve madencilik sektöründe kritik
öneme sahiptir.
• Pas giderici, yüzey temizleyici ve
cilalama maddesi olarak (örneğin paslanmaz çelik parlatmada). Asitle dağlama
(pickling) işlemlerinde kullanılır.
• Elektronik sanayinde yarı iletken
üretimi ve devre kartlarının temizlenmesinde ve mikroçip üretim süreçlerinde
kullanılır.
• Akvafortis olarak sanat/restorasyon
alanında, gravür ve baskı tekniklerinde kullanılır.
• Laboratuvar reaktifi olarak titrasyon,
analiz ve sentez işlemlerinde yaygın kullanılır.
• Nitrat tuzlarının üretiminde
kullanılır. Gümüş nitrat, baryum nitrat, potasyum nitrat gibi bileşiklerin
hazırlanmasında rol oynar.
• Kimyasal sentezlerde veya bazı
temizlik işlemlerinde güçlü oksidan olarak görev yapar.
• Özellikle kırmızı dumanlı nitrik asit
(RFNA) formunda, roket yakıtlarında oksitleyici bileşen olarak kullanılır.
• Altın ve diğer değerli metallerin
analizinde kullanılır. Altın ayar testinde, kral suyunun bir bileşeni olarak
kullanılır.
• Nitrik asit günlük hayatta okul
laboratuvarlarında kullanılan yaygın bir reaktiftir.
• Nitrik asit, gübre üretiminde amonyum
nitratlar üretmek için kullanılan önemli bir kimyasaldır.
• Kimyasal maddelerin imalatında plastik
yapımında ve boya üretiminde kullanılır.
• Metalurjide, cevher yüzdürmede ve
kullanılmış nükleer yakıtın yeniden işlenmesinde kullanılır.
• Nitrik asit sıvı yakıtlı roketlerde
oksitleyici olarak çeşitli şekillerde kullanılır (roket itici).
• Ayrıca tipik olarak bulanık su
numunelerinin, katı çamur numunelerinin element analizi gerektiren numune
türlerinin sindirim sürecinde de kullanılır.
DEPOLAMA
Nemden
uzak, kuru ve iyi havalandırılmış bir alanda sıkı ve kapalı kaplarda
depolanması gerekir. Ayrıca ayrışmayı önlemek için 0 °C'nin altında
saklanmalıdır.
NİTRİK
ASİT SATIŞI
ASR
Kimya olarak, İstanbul, İzmir, Bursa, Ankara, Kocaeli, Adapazarı, Sakarya,
Tekirdağ, Edirne, Çanakkale, Muğla, Gaziantep, Kahramanmaraş, Adana, Mersin,
Hatay, Konya, Kütahya, Kayseri, Samsun, Trabzon, Eskişehir, Yalova ve Rize gibi
Türkiye’nin doğudan batıya, kuzeyden güneye her iline nitrik asit toptan
satışını yapmaktayız.
Nitrik
asit nedir, nitrik asit nereden alınır, nitrik asit nerede satılır, nitrik asit
fiyatı, nitrik asit toptan fiyatı, nitrik asit satışı, nitrik asit toptan
satışı, nitrik asit nereden tedarik edilir gibi tüm soruların cevaplarını ASR
Kimyadan bulabilirsiniz.
GENEL BİLGİLER